La electroquímica no solo ha favorecido el avance de la investigación científica en estos últimos años, sino que nos ha ayudado con soluciones innovadoras para reducir los problemas ambientales que tiene nuestro ecosistema.
¿Qué es la electroquímica?
¿Qué tienen en común cargar la batería de un teléfono celular y evitar que una estructura metálica se oxide o deteriore con el tiempo? Ambos procesos dependen de la electroquímica. Esta rama interdisciplinaria de la química estudia las reacciones que permiten transformar la energía química en electricidad y utilizar la electricidad para generar cambios en la materia. Gracias a estos principios, hoy es posible alimentar dispositivos electrónicos, desarrollar tecnologías de almacenamiento de energía y diseñar soluciones innovadoras para la protección ambiental y el desarrollo sostenible.
Un poco de historia
La electroquímica tiene raíces que se remontan a la antigüedad. Existen hallazgos arqueológicos que algunos investigadores han interpretado como posibles dispositivos electroquímicos primitivos, como las llamadas “baterías de Bagdad”, estructuras compuestas por recipientes cerámicos, láminas metálicas y soluciones ácidas que datan de civilizaciones mesopotámicas. Aunque su uso exacto sigue siendo debatido y no existe consenso científico sobre si realmente funcionaron como baterías, estos descubrimientos evidencian que los materiales y configuraciones capaces de generar fenómenos electroquímicos han estado presentes en la historia humana desde tiempos remotos.
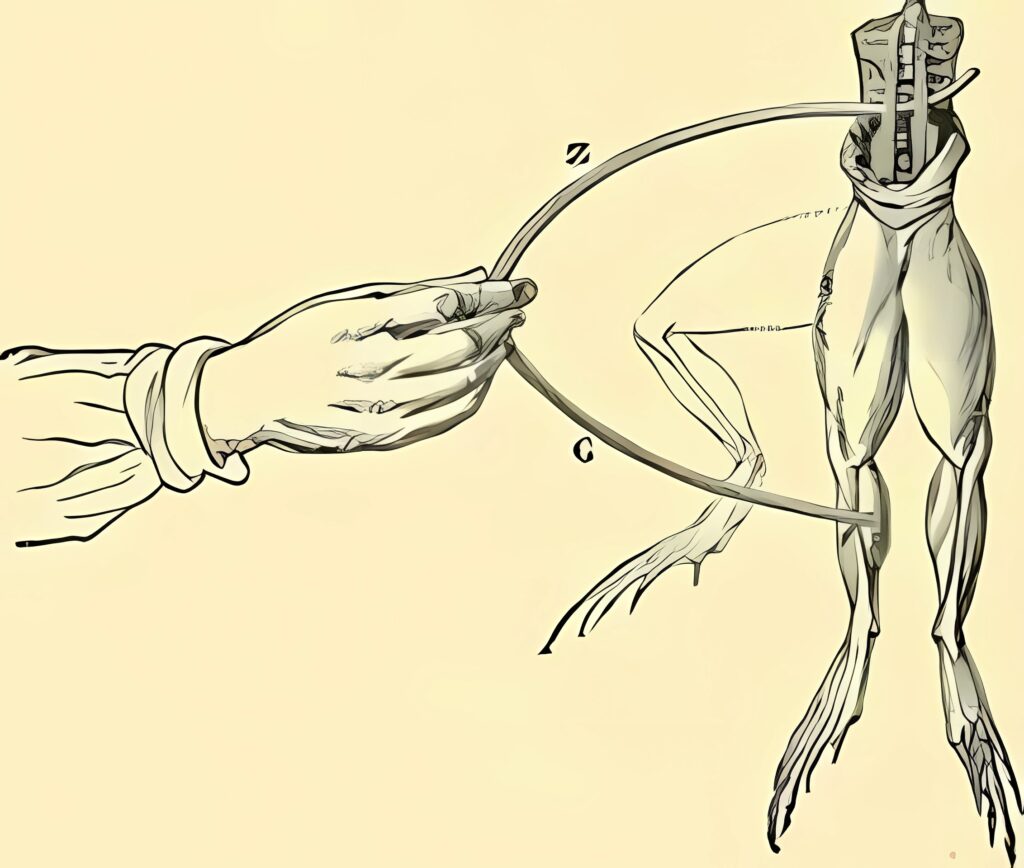
Sin embargo, el desarrollo formal de la electroquímica comenzó en el siglo XVIII. En 1786, el científico italiano Luigi Galvani observó que los músculos de las ranas se contraen al entrar en contacto con metales diferentes. A partir de estos experimentos propuso la existencia de una “electricidad animal”, lo que despertó gran interés en la comunidad científica y abrió el camino para el estudio sistemático de la relación entre electricidad y reacciones químicas.
Catorce años más tarde, en 1800, Alessandro Volta cuestionó la interpretación de Galvani y demostró que la electricidad no provenía del tejido animal, sino del contacto entre metales distintos en presencia de un medio conductor. Con base en este principio desarrolló la primera pila eléctrica, conocida como pila voltaica, considerada la primera fuente continua de corriente eléctrica estable de la historia convirtiéndose en un hito fundamental para el avance de la ciencia y la tecnología.
Sobre la base de estos descubrimientos, los científicos ingleses William Nicholson y Anthony Carlisle construyeron uno de los primeros sistemas electroquímicos funcionales utilizando una pila voltaica. Ese mismo año lograron descomponer el agua mediante el paso de corriente eléctrica a través de electrodos metálicos, observando la liberación de hidrógeno en un electrodo y oxígeno en el otro. Este fenómeno, conocido hoy como electrólisis del agua, demostró de manera experimental que la electricidad podía inducir reacciones químicas, consolidando así el nacimiento de la electroquímica como disciplina científica moderna.
Reacciones Químicas de Reducción y Oxidación: La base de su funcionamiento
Los electrones representan la carga negativa que presenta un átomo y las mismas que participan en la formación de enlaces químicos mediante el estado de oxidación de los elementos químicos. Cuando cambian los estados de oxidación de los elementos, dentro de una reacción química, ocurre una transferencia de electrones de una sustancia a otra, ya sea pérdida (oxidación) o ganancia (reducción), originando así el término de reacción de oxidación-reducción, o simplemente Redox.
Un ejemplo clásico de reacción Redox es la formación de cristales de plata a partir de la reacción entre cobre metálico y una solución de nitrato de plata. En este proceso, el cobre metálico se oxida al perder electrones y pasa a la solución como ion cobre, mientras que los iones plata presentes en la solución se reducen al ganar electrones y depositarse como plata metálica sólida.

La cantidad de electrones se debe a la carga que tienen los elementos, en estado iónico, para igualar la cantidad de cargas que tienen dentro de la reacción Redox. Además, las reacciones redox fueron de mucha importancia a lo largo de la historia y fueron tomadas como base para leyes que conocemos hoy en día.
La Ley de Faraday y su aplicación en la Electroquímica
Para ganar una entrada a la conferencia de Humphry Davy y aspirar a un puesto de trabajo en su laboratorio, Faraday inició sus estudios sobre la electrólisis, entendida como la descomposición de un compuesto en sus elementos mediante el uso de una corriente eléctrica. En este proceso, logró sistematizar el fenómeno de manera cuantitativa, estableciendo su relación con la intensidad de la corriente eléctrica aplicada a la celda electrolítica.
Con ese postulado, Faraday planteó las siguientes 2 leyes:
| 1. La masa de la sustancia liberada electroquímicamente es proporcional a la cantidad de electricidad que se hace pasar por la solución electrolítica. | 2. El peso del material liberado por una cantidad dada de electricidad es proporcional al peso equivalente del elemento de interés |
| m = (I*t*PM)/(n*F) | Peso equivalente = PM / n Equivalente electroquímico = m / F |
| Donde: m = masa depositada del metal de interés (g) I = intensidad de corriente del sistema (A) t= tiempo de reacción de electrólisis (s) PM = masa molecular del metal depositado (g/mol) n = estado de valencia del elemento F = constante de Faraday equivalente a 96500 Coulombs | Donde: PM = masa molecular del metal de interés (g/mol) n = estado de valencia del elemento Donde m = masa del metal de interés (g) F = constante de Faraday equivalente a 96500 Coulombs |
En la siguiente tabla, hay varios ejemplos de equivalente electroquímico, según los cambios de número de valencia de los metales.
Tabla 1. Equivalente electroquímico (×10⁻⁴ g/C)
| Ion | Símbolo | Cambio de carga (n e⁻ transferidos) | Equivalente |
| Oro (III) | Au³⁺ | Au³⁺ + 3e⁻ → Au (s) | 6.805 |
| Oro (I) | Au⁺ | Au⁺ + 1e⁻ → Au (s) | 20.41 |
| Hierro (III) | Fe³⁺ | Fe³⁺ + 3e⁻ → Fe (s) | 1.929 |
| Hierro (II) | Fe²⁺ | Fe²⁺ + 2e⁻ → Fe (s) | 2.894 |
| Cobre (II) | Cu²⁺ | Cu²⁺ + 2e⁻ → Cu (s) | 3.293 |
| Cobre (I) | Cu⁺ | Cu⁺ + 1e⁻ → Cu (s) | 6.585 |
Con base a esa ley, podemos obtener productos de manera industrial como el oxígeno gaseoso a partir de la electrólisis del agua, el recubrimiento de las tuberías con Niquel o Cromo, o en el uso de la metalurgia para joyería o bisutería.
Celda electroquímica: el sistema que permite las reacciones electroquímicas
Para que funcionen las reacciones electroquímicas, dentro de un proceso Redox, se necesita de las celdas electroquímicas, que son sistemas que emplean electricidad para generar reacciones químicas y viceversa, ya sea mediante reacciones de oxidación (pérdida de electrones) o reducción (ganancia de electrones).
Toda celda electroquímica está formada por componentes que permiten el movimiento controlado de electrones por un circuito externo y de iones dentro del sistema. Entre sus elementos principales se encuentran los que van a detallar a continuación:
- Electrodo: Son conductores eléctricos, generalmente metálicos o de materiales inertes como grafito o platino, que permiten el intercambio de electrones entre el circuito externo y la solución. En ellos ocurren las reacciones redox.
- Ánodo: Es el electrodo donde ocurre la oxidación, es decir, la pérdida de electrones. Desde este punto los electrones salen hacia el circuito externo. Su polaridad depende del tipo de celda: puede ser de tipo negativo o positivo según el sistema.
- Cátodo: Es el electrodo donde ocurre la reducción, es decir, la ganancia de electrones. En este punto los electrones ingresan desde el circuito externo hacia la celda. Al igual que el ánodo, su polaridad depende del tipo de celda.
- Solución electrolítica (electrolito): Es el medio que contiene iones libres capaces de transportar carga eléctrica dentro de la celda. Puede ser una solución acuosa o un electrolito fundido, y permite mantener el equilibrio de cargas mientras ocurre la reacción redox. En muchos sistemas también se emplean componentes adicionales, como puentes salinos o membranas, que facilitan el flujo de iones entre compartimentos y evitan la mezcla directa de reactivos.
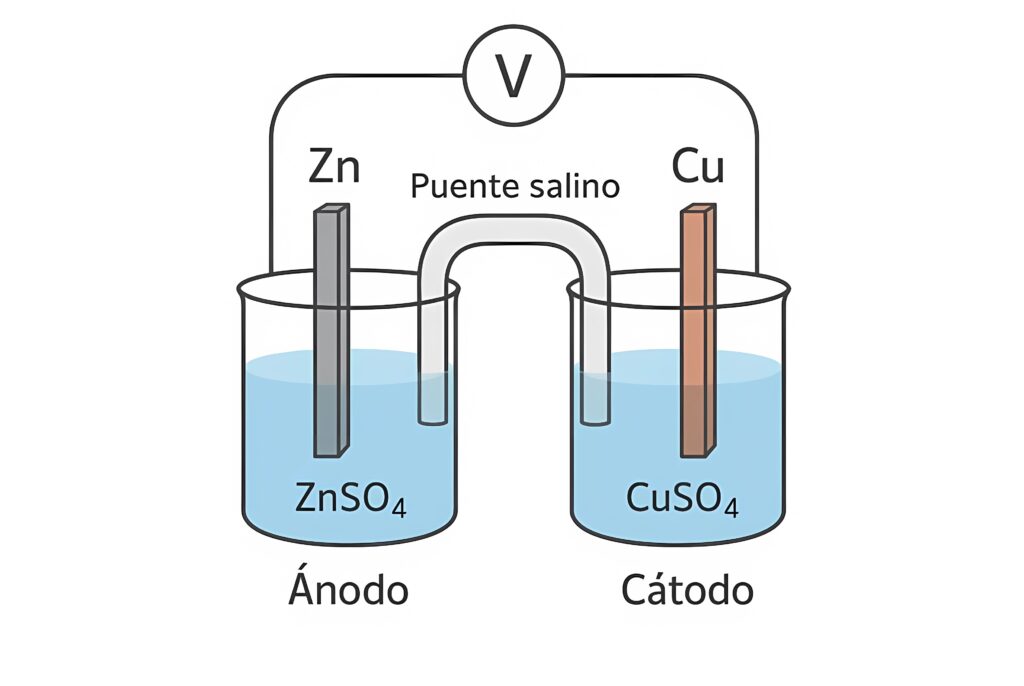
Según el tipo de reacción electroquímica, ya sea espontánea (reacción electroquímica genera electricidad) o no espontánea (necesidad de electricidad para generar una reacción electroquímica), tenemos 2 tipos de celdas electroquímicas descritas en la siguiente tabla con sus respectivos ejemplos. Ambos tipos de celdas constituyen el fundamento del almacenamiento de energía, según los procesos industriales electroquímicos y múltiples tecnologías orientadas al desarrollo sostenible:
Tabla No. 2: Tipos de celdas electroquímicas
| Tipo de celda | Descripción | Ejemplo |
| Celdas electrolíticas | Es un tipo de celda electroquímica que requiere de electricidad para impulsar una reacción electroquímica, en este caso la electrólisis (proceso de separación de compuestos mediante el uso de electricidad), en donde los cationes generados del ánodo se dirigen hacia el cátodo y viceversa con los aniones del cátodo hacia el ánodo. | La electro-obtención de cobre |
| Celdas galvánicas | Es un tipo de celda electroquímica que genera electricidad espontáneamente mediante una reacción electroquímica, en donde se necesita de un electrolito fuerte e inerte, como medio conductor, para que se lleve a cabo el proceso químico, y ver su fuerza electromotriz (o voltaje) en el que se da la reacción. | La celda de combustible |
La Electroquímica Analítica y sus soluciones para la sostenibilidad
A diferencia de las técnicas analíticas convencionales y en muchos casos, con un coste inversión algo elevado tales como la Espectrofotometría de Absorción Atómica (AAS) o la Cromatografía Iónica (IC), la Electroquímica Analítica engloba en sí varios métodos analíticos cualitativos y cuantitativos basados en las propiedades eléctricas de los analitos (en este caso los aniones y los cationes).
Además, la Electroquímica Analítica se diferencia de otras técnicas analíticas por su bajo costo de instrumentación, sus límites de detección competitivos o muy bajos y la especificidad hacia un estado de oxidación particular del elemento a analizar.
Con base a su instrumentación, el equipo de funcionamiento de la Electroquímica Analítica se compone de la siguiente manera: Los electrodos (trabajo, referencia y contraelectrodo), celda de trabajo, potenciostato y electrolito inerte.
Instrumentación
- Celda de trabajo
- Involucra un sistema electroquímico de 3 electrodos que minimiza los errores de voltaje, ocasionadas por las caídas de resistencia eléctrica mediante la solución electrolítica.
- Electrodos
- Electrodo de trabajo es de interés en nuestro análisis, en donde se va se va a realizar las reacciones Redox. Esta debe ser inerte para evitar interferencias químicas y su voltaje es medido en función del voltaje del electrodo de referencia. Se utiliza frecuentemente carbón vítreo, Diamante Dopado con Boro u otro material inerte.
- Electrodo de referencia tiene un potencial conocido que proporciona una referencia válida para hacer determinaciones electroquímicas. Se utiliza con frecuencia los de Plata/Cloruro de Plata y Calomelano
- Contraelectrodo ayuda al paso de la corriente eléctrica y cierra el circuito eléctrico de la celda electroquímica. Se utilizan con frecuencia los electrodos de grafito y platino.
- Potenciostato
- Es el instrumento clave para las determinaciones electroanalíticas que permite controlar el potencial del electrodo de trabajo y medir la corriente resultante con fines analíticos.
- Electrolitos
- Es una solución química que se añade en la celda electroquímica para evitar corrientes de migración en el sistema por el movimiento de partículas cargadas en el campo eléctrico.
Consideraciones de sostenibilidad en electroquímica analítica
Desde el punto de vista ambiental, la electroquímica analítica ha evolucionado hacia prácticas más sostenibles. Uno de los cambios más relevantes ha sido la sustitución progresiva del electrodo de calomelano, que contiene mercurio, por electrodos de referencia de plata/cloruro de plata, menos tóxicos y más seguros para el entorno.
Asimismo, el desarrollo de microelectrodos y ultramicroelectrodos ha permitido reducir el consumo de reactivos, mejorar la sensibilidad analítica y optimizar el transporte de masa hacia el electrodo de trabajo, contribuyendo a métodos más eficientes y ambientalmente responsables.
Sensores y biosensores electroquímicos: una chispa eléctrica para el desarrollo tecnológico
Una de las aplicaciones de la electroquímica analítica es la elaboración de sensores y biosensores, los cuales utilizan los principios de una celda electro analítica para la detección específica de analitos.
En términos generales, un sensor electroquímico es un dispositivo químico que no solo mide cambios de potencial (voltamétricos), sino mide otros parámetros eléctricos tales como corriente (amperométricos), conductividad (conductimétricos) e impedancia cuando una especie química interactúa con el analito, de manera excluyente y selectiva, para determinar su presencia, tanto cualitativa como cuantitativa. Podemos encontrar varios tipos de sensores electroquímicos y estos son los siguientes que se van a detallar:
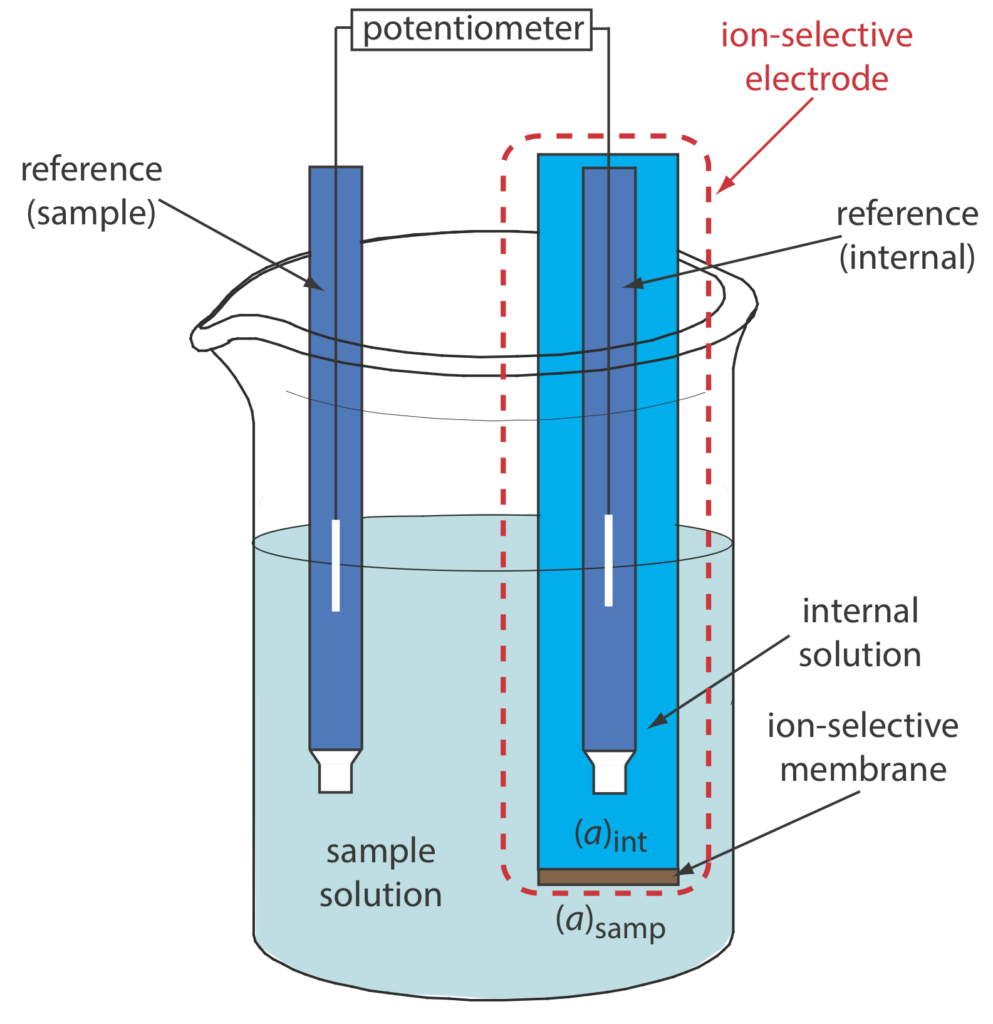
El electrodo de ión selectivo (EIS), que está basado en membranas permoselectivas que incluyen un elemento de reconocimiento químico que convierte la actividad del ión de interés en señal medida.
Los polímeros molecularmente impresos (MIP), basados de una síntesis por polimerización de un monómero funcional para que reaccione con la molécula de interés.
Electrodos modificados, que se fundamentan en la modificación del material original del sensor para mejorar o adaptar su respuesta. Un claro ejemplo es el electrodo selectivo al ion hidronio utilizado para la medición de pH en soluciones acuosas, actualmente conocido como el electrodo de vidrio.
Una variación de los sensores electroquímicos son los biosensores, que tiene el mismo principio de un sensor electroquímico común, solo que este se utiliza un elemento bioquímico o biológico (enzimas, bacterias, células, ácidos nucleicos, microorganismos) como sensor. Un ejemplo común es un medidor de glucosa para las personas con problemas de diabetes.
Lo común de estos sensores es que ambos tienen un transductor, que es un elemento instrumental que traduce la interacción sensor-analito diana (analito de interés) de la reacción electroquímica en señal analítica, en este caso eléctrica, hasta un dispositivo de medición y procesamiento de la información adquirida que queremos determinar.
El desarrollo de estos sensores da un enfoque multidisciplinario que nos permite explorar distintas áreas, para dar otras soluciones a los problemas que se nos presentan, tanto en el ámbito cotidiano como en el ámbito investigativo.
Descontaminación electrizante
Uno de los futuros para el tratamiento de aguas residuales es el uso de los Procesos de Oxidación Avanzada (POAs), que implican la formación electroquímica de los radicales hidroxilos (OHo), con un elevado potencial de oxidación para mineralizar los contaminantes, sobre todo los de tipo orgánico.
Cualquier contaminante orgánico, ya sea un pesticida, colorante o un fármaco emergente, estos se reducen a compuestos mineralizados (iones cloruro, nitratos, etc.) y evitan la formación de productos tóxicos que son dañinos al ecosistema, sobre todo al acuático por su difusión en el agua.
Conclusión
La electroquímica ha evolucionado mucho a lo largo de la historia, que no solo revolucionó en el ámbito del desarrollo tecnológico (como el desarrollo de sensores y biosensores), sino en el ámbito de sostenibilidad (uso de electrodos amigables con el medio ambiente) y la preservación de los recursos del Planeta Tierra (tratamiento de aguas mediante Procesos de Oxidación Avanzada).
Bibliografía de referencia
Alegret, S., del Valle, M., Merkoci, A. (2004). Sensores Electroquímicos Introducción a los quimiosensores y biosensores Curso teórico-práctico. Servei de Publicacions. Barcelona-España. Recuperado el 9 de Febrero de 2026, de: https://books.google.com.ec/books?hl=es&lr=&id=r39got4r0UgC&oi=fnd&pg=PA3&dq=transductor+sensores+electroquimicos&ots=QkrPuAmqcS&sig=2QbFR__dpRNwtEJa9fYHap_dz_c&redir_esc=y#v=onepage&q=transductor%20sensores%20electroquimicos&f=false
Baeza, A. (s.f.). Sensores y Biosensores Electroquímicos. Facultad de Química, Departamento de Química Analítica de la UNAM. Recuperado el 4 de Febrero del 2026, de: https://amyd.quimica.unam.mx/pluginfile.php/5834/mod_resource/content/0/Articulo_Sensores_y_Biosensores_2085.pdf
Ballesteros-Hernández, L., Contreras-Bárbara, J., Garza-Ortíz, A., Cervera-Castro, F., Hernández-Chávez, M. (2022). ¿Los culpables son los electrones? Una propuesta experimental a microescala de las reacciones redox. Revista Tendencias en Docencia e Investigación en Química 2022, 8 (8), 58 – 62. Recuperado el 4 de Febrero del 2026, de: https://zaloamati.azc.uam.mx/server/api/core/bitstreams/4a354fb7-ba23-4154-8274-45c9af3306f9/content
Burns, R. (2003). Fundamentos de Química. 4ta Edición. Pearson Educación. México.
Chamorro, G. y Jiménez, R. (2011). Purificación y Electrodeposición de Cobre a partir del Lixiviado de la empresa Ferroquímica S.R.L. para obtener cobre electrolítico a nivel laboratorio. Tesis para el título de Ingeniería Química de la Universidad Nacional del Centro de Perú, Recuperado el 9 de Febrero del 2026, de: https://repositorio.uncp.edu.pe/server/api/core/bitstreams/6b0e8fcf-a9b2-455a-aa0b-46be3d3e06a8/content
Conesa, J. (2021). Diseño de Reactores Avanzados. Recuperado el 4 de Febrero del 2026, de: https://es.scribd.com/document/788892404/REACTORES-EQ-2021
Fernández, R. (2016) Desarrollo del Sensor Electroquímico Basado en Electrodo de Carbón Vítreo Modificado con Polímero Molecularmente Impreso para la Determinación de Diuron en Muestra de Agua. Tesis para el título profesional de Licenciado en Química de la Universidad Nacional de Ingeniería. Recuperado el 9 de Febrero del 2016, de: https://repositorio.uni.edu.pe/bitstream/20.500.14076/5645/1/fernandez_cr.pdf
Flores, E. (1995). Voltametría cíclica: La Espectroscopía Electroquímica Parte I. Revista de Química, 9 (2), 165 – 172. Recuperado el 4 de Febrero del 2026, de: https://revistas.pucp.edu.pe/index.php/quimica/article/view/5564/5560
Garzón, L., Martínez, Y., Aristizabal, C. (2014). Historia de la Electroquímica en la Formación Inicial de Profesores, Una Experiencia Investigativa. III Conferencia Latinoamericana del International, History and Philosophy of Science Teaching Group IHPST – LA 2014, 357 – 367. Recuperado el 4 de Febrero del 2026, de: https://www.researchgate.net/profile/Andrea-Martinez-Becerra/publication/339297967_HISTORIA_DE_LA_ELECTROQUIMICA_EN_LA_FORMACION_INICIAL_DE_PROFESORES_UNA_EXPERIENCIA_INVESTIGATIVA/links/5e4966b7458515072da44bb3/HISTORIA-DE-LA-ELECTROQUIMICA-EN-LA-FORMACION-INICIAL-DE-PROFESORES-UNA-EXPERIENCIA-INVESTIGATIVA.pdf
González, C. (2019). Solución al problema de Fuga en Celdas Electroquímicas Microfluídas mediante la Variación del ancho del Electrodo. Tesis de Maestría en Electroquímica del Centro de Investigación y Desarrollo tecnológico en Electroquímica CONACYT. Recuperado el 4 de Febrero del 2026, de: https://cideteq.repositorioinstitucional.mx/jspui/bitstream/1021/411/1/TESIS%20CARLOS%20LUIS%20GONZ%c3%81LEZ%20GALLARDO.%20MAE%20r.pdf
Iglesias, A. (2015). Determinación Electroquímica del Sulfametoxazol. Tesis de fin de Máster en la Universidad de Burgos. Recuperado el 4 de Febrero de 2026, de: https://riubu.ubu.es/bitstream/handle/10259/3817/Iglesias_Garc%c3%ada.pdf?sequence=1&isAllowed=y
Larmat, F. (2022). Sensores Electroquímicos: Teoría y Aplicaciones. 1ra Edición. Universidad del Valle. Cali-Colombia. Recuperado el 9 de Febrero del 2026, de: https://books.google.com.ec/books?hl=es&lr=&id=lffNEAAAQBAJ&oi=fnd&pg=PA9&dq=sensores+electroquimicos+tipos+&ots=gv3nmP-Pgt&sig=G7ohLC8YRdIouIR2aySK9ulKsN0&redir_esc=y#v=onepage&q=sensores%20electroquimicos%20tipos&f=false
Morales, A. (2003). Electrometalurgia. Apunte para alumnos de Ingeniería Metalúrgica. Departamento de Ingeniería Metalúrgica de la Universidad Católica del Norte. Recuperado el 4 de Febrero del 2026, de: https://bluebooksoft.com/METALURGIA/2148.pdf
Muñoz, J. (2019). Automatización de un Banco de Pruebas de una Celda Electroquímica. Tesis del Programa de Ingeniería Mecatrónica de la Universidad Autónoma de Bucaramanga. Recuperado el 4 de Febrero del 2026, de: https://repository.unab.edu.co/bitstream/handle/20.500.12749/7082/2019_Tesis_Juan_Pablo_Mu%c3%b1oz_Vidal.pdf?sequence=1&isAllowed=y
Navas, C. (2018). Uso del experimento de la electrólisis del agua para la enseñanza de conceptos básicos de electroquímica y la introducción al nuevo sistema internacional de unidades a estudiantes de grado once: un enfoque basado en la Enseñanza para la Comprensión. Tesis de Máster en Enseñanza de las Ciencias Exactas y Naturales de la Universidad Nacional de Colombia. Recuperado el 9 de Febrero del 2026, de: https://bffrepositorio.unal.edu.co/server/api/core/bitstreams/48d93494-77a5-4e2e-bf6d-93427b8ab786/content
Pediaexpertos. (s.f.). Diferencia entre celda galvánica y electrolítica. Recuperado el 4 de Febrero del 2026, de: https://pediaexpertos.com/diferencia-entre-celda-galvanica-y-electrolitica/
Poveda, G. (2010). Dos siglos de Electroquímica. 1ra Edición. Colección Memoria de los Ingenieros. Medellín – Colombia. Recuperado el 4 de Febrero del 2026, de: https://repositorio.itm.edu.co/server/api/core/bitstreams/089cd1fb-d9e0-4e1b-8efe-45703df592b7/content
Rincón, J. y Abello, S. (2017). Análisis de la deposición electrogravimétrica del cobre y su aplicación en recubrimientos niquelados. Formato sciencia et tcenica. Recuperado el 9 de Febrero del 2026, de: https://d1wqtxts1xzle7.cloudfront.net/52281190/Analisis_de_la_deposicion_electrogravimetrica_del_cobre_y_su_aplicacion_en_recubrimientos_niquelados-libre.pdf?1490314605=&response-content-disposition=inline%3B+filename%3DAnalisis_de_la_deposicion_electrogravime.pdf&Expires=1770701205&Signature=C3AXOHtMJLjVp6Ss3jEHuVzULBiGBVU317pzZcWek9A2unEjK3DDbE-ciJ2Rxao~1zJ1kf0wkn528ZeTQShDB3LFIGJpPuDtO-Yu34L4~93TD9yxOw4e5vjIkW1gGXZ-sLJepMHNlyTtBKdQZKpIWVgFrgFZKFsAWuQ56qgQlT-~nVXeLp463meBmBVe56o4nSOx-Ncn98w5Z2Lctd7X–dUlgMb-1DKqBqj116VNC5nhXAInysIYyq1qga7RMIdvkVNZaxvaz1pu-cTmK5HrJ64vE0H9T7FJqgPiXVLgxhZSbBX-QH9a3i9ao7HjCBf7TZtGnid3C2JhqsKhMwJ3w__&Key-Pair-Id=APKAJLOHF5GGSLRBV4ZA
Rodríguez, G. (1994). La Naturaleza eléctrica de la materia. Boletín PPDQ de la Universidad Pedagógica Nacional. Recuperado el 9 de Febrero de: https://revistas.upn.edu.co/index.php/PPDQ/article/view/24198/15345
Rufino, L. y Pereira, C (2021). Grado de Remoción de Colorantes en los Efluentes Flexo Gráficos, empleando un método combinado Electro catálisis – Oxidación Avanzada. Informe final de Investigación de la Universidad Nacional de Callao. Recuperado el 4 de Febrero del 2026, de: https://repositorio.unac.edu.pe/backend/api/core/bitstreams/985b239f-a0ff-4da0-84b7-92567cb21851/content
Viltres, M. (2019). Nuevos electrodos selectivos a iones Pb (II) basados en aroiltioureas 3,3-dimetil sustituidas. Tesis de Máster en Ciencia y Tecnología de los Materiales de la Universidad de La Habana. Recuperado el 9 de Febrero de 2026, de: https://accesoabierto.uh.cu/files/original/2130724/Marcia_Viltres_Portales.pdf
Zinola, F. (2007). Electroquímica Fundamental y Aplicaciones. 2da Edición. Edición DIRAC. Facultad de Ciencias de la Universidad de la República. Montevideo, Uruguay. Recuperado el 4 de Febrero del 2026, de: https://eva.fcien.udelar.edu.uy/pluginfile.php/51794/mod_resource/content/1/Electroqu%C3%ADmica%20Fundamental%20y%20Aplicaciones%20LIBRO.pdf

